Công thức tính độ đậm đặc Phần Trăm là dạng đo lường và được học tập vô công tác Hóa học tập ở cấp cho trung học tập hạ tầng. Tuy nhiên, vô cuộc sống đời thường giống như việc làm từng ngày thì công thức này đều được tất cả chúng ta vận dụng thông thường xuyên.
Bạn đang xem: Công thức tính nồng độ phần trăm - Thuật toán đơn giản, dễ áp dụng
Nước sạch sẽ đem thiệt sự “sạch”, QUÁ KINH HÃI với những hình hình họa thực tiễn đằng sau
Công thức tính độ đậm đặc phần trăm
1. Nồng chừng Phần Trăm là gì?
Nồng chừng Phần Trăm (C%) của một hỗn hợp là độ đậm đặc thể hiện tại mang lại tớ biết số gam hóa học tan đem vô 100 gam hỗn hợp.

Công thức tính độ đậm đặc Phần Trăm được dùng thật nhiều vô hóa học
2. Cách tính độ đậm đặc phần trăm
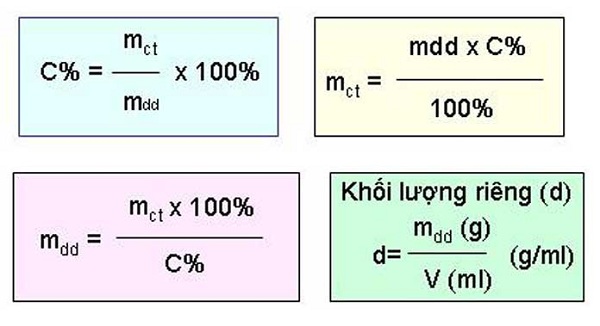
C% = mct/cdd.100%
Trong đó:
C%: Nồng chừng phần trăm
mct: Khối lượng hóa học tan
mdd: Khối lượng hỗn hợp ( mdd= m dung môi + m hóa học tan).
Các công thức suy rời khỏi từ công thức tính độ đậm đặc phần trăm
Công thức tính lượng hóa học tan: mct = (C%*mdd)/100%
Công thức tính lượng dung dịch: mdd = (mct*100%)/C%
MỜI BẠN THAM KHẢO DANH SÁCH MÁY LỌC NƯỚC GIÁ RẺ VÀ CHẤT LƯỢNG NHẤT TRÊN THỊ TRƯỜNG
3. Bài luyện vận dụng tính công thức độ đậm đặc Phần Trăm (C%)
Ví dụ 1: Hòa tan 10 gam đàng vô 40 gam nước. Hãy tính nồng chừng Phần Trăm của hỗn hợp nhận được.
-Tính lượng của dung dịch
Ta có: mdd= mdm + mct = 10+ 40= 50 gam (mdm là lượng dung môi)
-Nồng chừng phần trăm:
C%= mct/mdd. 100%= (10/50).100%= 20%
Ví dụ 2: Cho hỗn hợp H2SO4 đem độ đậm đặc 28%. Tính lượng H2SO4 đem vô 300 gam hỗn hợp.
Xem thêm: Tử vi tuổi Mùi năm 2024: Sự nghiệp thăng hoa, tiền bạc ồ ạt chảy về túi
– Khối lượng của H2SO4 đem vô 300 gam dung dịch:
m = (28 x 300)/100 = 84 (gam)
Công thức tính độ đậm đặc Phần Trăm giản dị, dế hiểu
Công thức tính độ đậm đặc mol của hỗn hợp (Cm)
Nồng chừng Mol là định nghĩa quen thuộc với bọn chúng ta
1. Khái niệm độ đậm đặc mol
Nồng chừng mol (CM) của hỗn hợp là đại lượng mang lại tớ biết số mol hóa học tan đem trong một lít hỗn hợp.
2. Công thức tính độ đậm đặc mol
CM = n/V (đơn vị: mol/l)
Trong đó:
- n: số mol hóa học tan
- V: thể tích hỗn hợp (lít)
- Đơn vị mol/l còn được viết lách là M.
Từ công thức tính nồng chừng Phần Trăm của dung dịch tớ rất có thể suy rời khỏi hàng loạt những công thức sau:
Số mol hóa học tan: n = Cm . Vdd ( mol)
Thể tích dung dịch: Vdd= nCm( lít)
Qùa tặng ebook không tính phí – 100 thắc mắc – đáp về nước và tay nghề xương huyết rửa sạch mối cung cấp nước. Để có được không thiếu thốn ebook này, Shop chúng tôi ham muốn chào chúng ta ĐK vấn đề của tớ bằng phương pháp điền vô kiểu ĐK tiếp sau đây. Đăng ký là trọn vẹn không tính phí và nhanh chóng chóng
Đăng ký là trọn vẹn không tính phí và nhanh chóng chóng
3. Một số bài xích luyện vận dụng
– Ví dụ : Trong 250 ml dd đem hòa tan 16g CuSO4. Tính độ đậm đặc mol của hỗn hợp bên trên.
⇒ Số mol CuSO4 vô hỗn hợp là:
nCuSO4 = 16/160 = 0,1 (mol)
⇒ Nồng chừng mol của hỗn hợp CuSO4 là:
CM = 0,1/0,25 = 0,4 (mol/l)
Xem thêm: Trung Tâm Thuốc Central Pharmacy
Công thức tính độ đậm đặc phần trăm được vận dụng nhiều trong các công việc phân tích những công thức, phản xạ chất hóa học. Nắm được những công thức này sẽ không những mang lại lợi ích mang lại tất cả chúng ta vô việc làm mà còn phải vô cuộc sống đời thường, học hành từng ngày.
MỜI BẠN THAM KHẢO DANH SÁCH MÁY LỌC NƯỚC GIÁ RẺ VÀ CHẤT LƯỢNG NHẤT TRÊN THỊ TRƯỜNG
Post Views: 128.853











Bình luận