KClO3 → KCl + O2 là phản xạ phân bỏ. Bài viết lách này cung ứng không thiếu thốn vấn đề về phương trình chất hóa học và được thăng bằng, ĐK những hóa học nhập cuộc phản xạ, hiện tượng kỳ lạ (nếu có),bên cạnh đó tất nhiên một số trong những bài bác tập luyện tương quan sở hữu đáp án. Từ cơ, canh ty những em nắm rõ kỹ năng phần này. Mời chúng ta đón xem:
Phản ứng KClO3 → KCl + O2
Bạn đang xem: KClO3 → KCl + O2 | KClO3 ra KCl | KClO3 ra O2
1. Phương trình nhiệt độ phân KClO3
2KClO3 2KCl + 3O2
2. Điều khiếu nại phản xạ KClO3 rời khỏi KCl
Nhiệt độ
3. Bản hóa học của KClO3 (Kali clorat) nhập phản ứng
Ở nhiệt độ chừng 500℃ KClO3 bị phân bỏ trở nên muối bột kali clorua và oxI. Phản ứng này trọn vẹn hoàn toàn có thể xẩy ra ở nhiệt độ chừng thấp rộng lớn nếu như dùng MnO2 thực hiện hóa học xúc tác.
4. Mở rộng lớn về KClO3
4.1.Tính Hóa chất của kali clorat
Là một hóa học lão hóa mạnh, hoàn toàn có thể thuộc tính với tương đối nhiều phi kim và sắt kẽm kim loại như cacbon, photpho, nhôm, lưu hoàng, magie,…
2KClO3 + 3S → 2KCl + 3SO2
KClO3 + 3Mg → KCl + 3MgO
5KClO3 + 6P → 5KCl + 3P2O5
Các phương trình phản xạ khác:
KClO3 + 6HCl → 3Cl2 + KCl + 3H2O
2KClO3 + 3MnO2→ 2KMnO4 + MnCl2 + 2O2
KClO3 + 3H2 → KCl + 3H2O
4.2. Điều chế kali clorat như vậy nào?
Có nhiều phương pháp để pha trộn Kali Clorat, rõ ràng là:
Đun giá Canxi Clorat với muối bột Kali Clorua ở nhiệt độ chừng 70 – 75 °C
2KCl + Ca(ClO3)2 ⟶ 2KClO3 + CaCl2
Cho Kali Clorua thuộc tính với Natri Clorat ở ĐK thường
KCl + NaClO3 ⟶ KClO3 + NaCl
Điện phân hỗn hợp Kali Cloria ko vách ngăn nhập ĐK nhiệt độ chừng 70°C. Phản ứng tiếp tục thực hiện lớp bọt do khí tạo ra H2 xuất hiện tại.
H2O + KCl ⟶ H2 + KClO3
Cho Bari Clorat thuộc tính với Kali iodat ở ĐK thông thường. Phản ứng xẩy ra như sau:
Ba(ClO3)2 + 2KIO3 ⟶ 2KClO3 + Ba(IO3)2
Nhiệt phân Kali hypoclorit nhập ĐK nhiệt độ chừng 70°C. Phản ứng xẩy ra như sau:
3KClO ⟶ 3KCl + KClO3
4.3. Ứng dụng của Kali clorat – KClO3
- Được trộn lẫn lộn với tương đối nhiều loại vật tư dễ dàng cháy như lưu hoàng, photpho, bột sắt kẽm kim loại,… nhằm sản xuất dung dịch nổ, phát hành pháo bông, ngòi nổ..
- Dùng nhằm phát hành diêm: Thuốc ở đầu que diêm thông thường chứa chấp ngay gần 50% Kali Clrorat.
- Điều chế oxy nhập chống thực nghiệm bằng phương pháp nhiệt độ phân KClO3 với xúc tác là MnO2.
- Dùng thực hiện hóa học khử màu sắc nhập đan nhuộm và hóa học chống lão hóa.
- Kali Clorat là 1 hóa học sở hữu tính lão hóa cực mạnh, Khi bị lão hóa tiếp tục hóa giải khí oxy nên nó hoàn toàn có thể sử dụng như 1 hóa học khử cỏ.
- Tại nước ta, muối bột Kali Clorat được dùng như 1 hóa học điều tiết cây cối nhập nông nghiệp.
Cho Kali hydroxit KOH thuộc tính với khí Clo ở nhiệt độ chừng bên trên 80 chừng C. Phản ứng xẩy ra như sau:
3Cl2 + 6KOH ⟶ 3H2O + 5KCl + KClO3
5. Bài tập luyện vận dụng
Câu 1. Ứng dụng của KClO3 là
A. Chế tạo nên dung dịch nổ, phát hành pháo bông, ngòi nổ và những lếu thích hợp dễ dàng cháy không giống.
B. Dùng nhập công nghiệp diêm.
C. Dùng nhằm pha trộn oxi nhập chống thực nghiệm bên dưới dạng phản xạ nhiệt độ phân và sở hữu hóa học xúc tác là MnO2.
D. Tất cả những đáp án bên trên.
Lời giải:
Đáp án: D
Một số phần mềm của KClO3 là:
- Chế tạo nên dung dịch nổ, phát hành pháo bông, ngòi nổ và những lếu thích hợp dễ dàng cháy không giống.
- Dùng nhập công nghiệp diêm.
- Dùng nhằm pha trộn oxi nhập chống thực nghiệm bên dưới dạng phản xạ nhiệt độ phân và sở hữu hóa học xúc tác là MnO2.
Câu 2. Tổng thông số của toàn bộ những hóa học nhập phương trình sau:
KClO3 KCl + O2
A. 2
B. 4
C. 7
D. 5
Lời giải:
Đáp án: C
PTHH: 2KClO3 2KCl + 3O2
⇒ Tổng thông số là 7.
Câu 3. Khi nói tới tài năng phản xạ của oxi, đánh giá sai là
A. Oxi phản xạ thẳng với đa số những sắt kẽm kim loại.
B. Oxi phản xạ thẳng với toàn bộ những phi kim.
C. Oxi nhập cuộc nhập những quy trình xẩy ra sự hóa học, sự han gỉ, sự thở.
D. Những phản xạ tuy nhiên oxi nhập cuộc đều là phản xạ lão hóa – khử.
Lời giải:
Đáp án: B
Nhận xét sai là: Oxi phản xạ thẳng với toàn bộ những phi kim.
Vì oxi ko phản xạ thẳng với những halogen
Câu 4. Nhiệt phân trọn vẹn 12,25 g KClO3 thu được khí oxi. Tính thể tích của khí nhận được ở đktc là
A. 3,36 lít
B. 2,24 lít
C. 3,2 lít
D. 4,8 lít
Lời giải:
Xem thêm: 20 cách điều trị nám tàn nhang hiệu quả và nhanh chóng
Đáp án: A
Vậy = 0,15. 22,4 = 3,36 lít
Câu 5. Cho sơ đồ dùng sau: KClO3 + C KCl + X. Chất X là
A. CO2
B. Cl2
C. CO
D. O2
Lời giải:
Đáp án: A
2KClO3 + 3C 2KCl + 3CO2
Câu 6. Cho phương trình phản xạ chất hóa học sau:
2KClO3 + 3C 2KCl + 3CO2
KClO3 đóng tầm quan trọng gì?
A. Chất khử
B. Vừa là hóa học khử một vừa hai phải là hóa học oxi hóa
C. Chất oxi hóa
D. Chất môi trường
Lời giải:
Đáp án: C
KClO3 đóng tầm quan trọng là hóa học lão hóa vì thế số lão hóa của Clo rời kể từ +5 xuống -1.
Câu 7. Cho 1,2 gam C thuộc tính không còn với KClO3 thu được V lít khí X ở đktc. Giá trị của V là
A. 2,24
B. 3,36
C. 4,48
D. 8,96
Lời giải:
Đáp án: A
2KClO3 + 3C 2KCl + 3CO2
= 0,1 mol
V = 0,1. 22,4 = 2,24 lít
Câu 8. Nhỏ kể từ từ hỗn hợp HCl quánh nhập ống thử chứa chấp KClO3 hiện tượng xẩy ra là
A. Không sở hữu hiện tượng kỳ lạ gì
B. Xuất hiện tại kết tủa trắng
C. Có khí gold color lục bay ra
D. Có Khi gray clolor đỏ hỏn bay ra
Lời giải:
Đáp án: C
6HCl + KClO3 → 3Cl2↑ + KCl + 3H2O
⇒ Có khí gold color lục (Cl2) bay rời khỏi.
Câu 9. Ứng dụng này tại đây không phải của KClO3?
A. Sản xuất diêm.
B. Điều chế oxi nhập chống thực nghiệm.
C. Sản xuất pháo bông.
D. Chế tạo nên dung dịch nổ đen thui.
Lời giải:
Đáp án: D
được phần mềm nhằm sản xuất dung dịch nổ, diêm, phát hành pháo bông, ngòi nổ và những lếu thích hợp dễ dàng cháy.
còn được dùng làm pha trộn oxi nhập PTN.
Chọn D vì thế bộ phận của dung dịch nổ đen thui là , C và S.
Câu 10. Nhiệt phân trọn vẹn 2,45 g KClO3 nhận được O2. Cho Zn thuộc tính không còn với lượng oxi một vừa hai phải nhận được, tính lượng oxit nhận được sau phản ứng?
A. 2,45 g
B. 5,4 g
C. 4,86 g
D. 6,35 g
Lời giải:
Đáp án: C
Khối lượng oxit nhận được sau phản xạ là:
Xem thêm thắt những phương trình chất hóa học khác:
P + KClO3 → KCl + P2O5 | P.. rời khỏi P2O5
KClO3 + HCl → Cl2 + KCl + H2O | KClO3 rời khỏi Cl2
Xem thêm: Thẻ tín dụng Super Shopee Platinum: Freeship cả năm, 365 ngày hoàn tiền | VPBank
Cl2 + KOH → KCl + KClO3 + H2O | Cl2 rời khỏi KClO3
KCl + H2O → KOH + H2 + Cl2 | KCl rời khỏi Cl2
H2SO4 + KCl → HCl + K2SO4 | KCl rời khỏi HCl
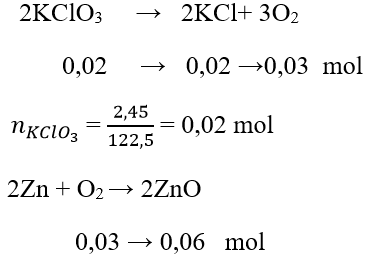









![#1 [Báo Giá] Bình ắc quy GS 12V 100Ah - Chính Hãng, Giá Tốt](https://muaacquy.vn/uploads/images/603e0553485ca4140f15bd03/ac-quy-gs-n100-12v-100ah.png)

Bình luận